
Po raz pierwszy w IPPT PAN świętowano Międzynarodowy Dzień Fizyki Medycznej. Obchody miały na celu popularyzowanie tematyki związanej z fizyką medyczną, ukazanie relacji pomiędzy nowoczesną technologią a efektami terapii oraz pokazanie wkładu własnego IPPT PAN w badania i w rozwój zaawansowanych technologii medycznych. Fizyk medyczny nie jest lekarzem, ale jego rola w medycynie jest bardzo ważna – bez ścisłej współpracy lekarza i fizyka medycznego leczenie często nie byłoby skuteczne.
Międzynarodowy Dzień Fizyki Medycznej obchodzono w dniu 7 listopada 2019 roku w dwóch jednostkach IPPT PAN: w Zakładzie Ultradźwięków IPPT PAN (zajęcia popularnonaukowe prowadzone były przez dr inż. Hannę Piotrzkowską-Wróblewską) oraz w Samodzielnej Pracowni Polimerów i Biomateriałów (dr inż. Tomasz Kowalczyk).
 |
 |
Międzynarodowy Dzień Fizyki Medycznej to święto, które obchodzone jest od 2013 roku z inicjatywy Międzynarodowej Organizacji Fizyki Medycznej zrzeszającej 88 narodowych Towarzystw Fizyków Medycznych i ma na celu promować zagadnienia związane z fizyką medyczną. Międzynarodowy Dzień Fizyki Medycznej obchodzono w IPPT PAN po raz pierwszy, ale IPPT PAN posiada wieloletnie doświadczenie w zakresie fizyki medycznej.
PRZYKŁADY TEMATYKI BIEŻĄCYCH BADAŃ PROWADZONYCH W IPPT PAN
I ZWIĄZANYCH Z FIZYKĄ MEDYCZNĄ
W ZAKŁADZIE ULTRADŹWIĘKÓW Instytutu Podstawowych Problemów Techniki PAN realizowane są obecnie trzy nurty badań naukowych:
1) Zastosowanie ultrasonografii ilościowej w diagnostyce zmian ogniskowych piersi oraz monitorowanie odpowiedzi guzów piersi na chemioterapię.
Ultrasonografia (USG) jest jednym z podstawowych badań lekarskich w diagnostyce chorób nowotworowych piersi. Uzupełnieniem tradycyjnego obrazowania ultradźwiękowego jest analiza surowych ech ultradźwiękowych RF (tzw. ultrasonografia ilościowa). Technika ta umożliwia pozyskanie dodatkowych informacji na temat cech morfologicznych badanej tkanki. Dane takie, pozwalają w sposób nieinwazyjny (bez konieczności wykonywania biopsji i oceny histopatologicznej tkanki) m. in. na ocenę stopnia złośliwości guza i na ocenę skutków chemioterapii . Dzięki poprawnej diagnozie na wczesnym etapie, możliwe jest zaplanowanie skutecznej terapii, co w konsekwencji pozytywnie wpływa na rokowanie pacjenta i zwiększa szanse na całkowite wyleczenie i przeżycie. Monitorowanie chemioterapii przyczynia się do zwiększenia liczby zabiegów oszczędzających pierś i pozwala na szybką zmianę terapii w przypadku opornych guzów.
Badania prowadzone są w Zakładzie Ultradźwięków przy współpracy z Centrum Onkologii im. Marii Skłodowskiej-Curie w Warszawie.
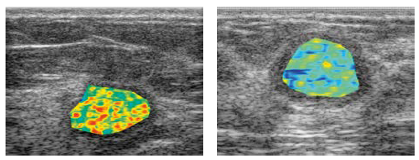
Ryc. 1. Ultradźwiękowe mapy ilościowe dwóch typów nowotworów: zmiana rakowa (po lewej stronie) oraz zmiana łagodna (po prawej stronie), charakteryzowane za pomocą biomarkera określanego mianem entropii.
2) Nanocząstki magnetyczne w polu ultradźwiękowym i magnetycznym jako sensybilizatory (uczulacze) termiczne
Nanocząstki magnetyczne są obecnie szeroko stosowane zarówno w terapii jak i diagnostyce medycznej. Głównym obszarem badań prowadzonych w Zakładzie Ultradźwięków jest badanie magnetycznych nanocząstek jako czynnika podnoszącego wydajność tzw. lokalnej hipertermii, tj. miejscowego wzrostu temperatury tkanki m.in.. w celu niszczenia nowotworów. Głównym celem badań jest ocena jakości hipertermii ultradźwiękowej i magnetycznej oraz znalezienie powiązań pomiędzy działaniem obu pól w obecności nanocząstek magnetycznych. Badanie nowatorskiej hipertermii dualnej, wywołanej równoczesnym działaniem zmiennego pola magnetycznego i ultradźwiękowego, wymaga specjalistycznego sprzętu pomiarowego. Stanowisko pomiarowe, umożliwiające pomiar wielkości efektu wzrostu temperatury w dualnej hipertermii skonstruowano w Zakładzie Ultradźwięków.

Ryc. 2. Stanowisko pomiarowe do badania efektów termicznych działania dualnej hipertermii ultradźwiękowo-magnetycznej.
3) Termiczne niszczenie litych guzów za pomocą zogniskowanych fal ultradźwiękowych
W ostatnich latach pojawiły się nowe podejścia terapeutyczne do leczenia litych guzów nowotworowych za pomocą zogniskowanych fal ultradźwiękowych (FUS). Technologia oparta na FUS - to nieinwazyjna (bez ingerencji chirurgicznej) technika umożliwiająca termiczne niszczenie zarówno pierwotnych litych guzów jaki i ich przerzutów zlokalizowanych głęboko pod skórą. Podstawową zaletą tego typu terapii jest brak jonizacji, znaczące zmniejszenie skutków ubocznych po terapii, możliwość jej wielokrotnego powtarzania oraz skrócenie czasu rekonwalescencji w porównaniu z konwencjonalnumi metodami leczenia (chirurgia, radio- i / lub chemioterapia).
Terapia wykorzystująca FUS o niskim lokalnym natężeniu polega na hipertermii (41÷43 °C) patologicznych tkanek. Podczas terapii wrażliwe na temperaturę liposomy wypełnione cytotoksycznym lekiem są dostarczane selektywnie do guza. Uwolnienie leku następuje poprzez pękanie liposomalnych mikropęcherzyków wywołane padającymi na nie falami ultradźwiękowymi. W przypadku terapii z użyciem FUS o wysokim lokalnym natężeniu następuje termoablacyjne zniszczenie samego guza, nie uszkadzając otaczających go zdrowych tkanek.

Aktywność SAMODZIELNEJ PRACOWNI POLIMERÓW I BIOMATERIAŁÓW (SPPiB) łączy w sobie badania podstawowe oraz działania o charakterze aplikacyjnym, które nabierają coraz większego znaczenia w odpowiedzi na wyzwania współczesnego świata. Prowadzone w SPPiB badania wpisują się w oczywiste i odwieczne dążenie ludzi do długiego życia w jak najlepszym zdrowiu, które to dążenie jest siłą napędową pracy ogromnej rzeszy naukowców, lekarzy i farmaceutów na całym świecie. Na obecnym etapie rozwoju cywilizacji, wydłużanie życia i poprawa stanu zdrowia wymaga sięgania po coraz bardziej skomplikowane - niekonwencjonalne rozwiązania, leżące na pograniczu różnych dziedzin, czego dobrym przykładem jest dynamicznie rozwijająca się inżynieria tkankowa, będąca interdyscyplinarną nauką łączącą wiedzę z zakresu biologii i medycyny z osiągnięciami inżynierii materiałowej, fizyki i chemii w celu wytwarzania funkcjonalnych zamienników uszkodzonych tkanek lub całych narządów.
Aktywność SPPiB jest skoncentrowana na szeroko rozumianych zagadnieniach inżynierii tkankowej, z naciskiem na biodegradowalne polimerowe rusztowania (ang. scaffolds), służące do regeneracji uszkodzonych tkanek. Podejmowane w SPPiB badania obejmują szerokie spektrum materiałów polimerowych, od naturalnych po syntetyczne, włączając w to szeroką gamę mieszanek polimerowych oraz materiałów kompozytowych. Pracownia wykorzystuje różnorodne procesy formowania rusztowań komórkowych, takie jak elektroprzędzenie struktur nanowłóknistych, druk 3-D czy też opracowywanie wstrzykiwalnych hydrożeli. Wzorem dla tworzonych rusztowań jest naturalnie występująca trójwymiarowa macierz zewnątrzkomórkowa (ECM), stanowiąca środowisko w którym funkcjonują komórki. Prowadzona optymalizacja procesowo-materiałowa ma na celu stworzenie możliwie korzystnego środowiska dla żywych komórek, z perspektywy ich adhezji, migracji, proliferacji, czy też różnicowania się w przypadku użycia komórek macierzystych. W obszarze zainteresowań SPPiB leżą też biodegradowalne materiały polimerowe jako systemy kontrolowanego uwalniania leków. Optymalizacja kinetyki uwalniania substancji aktywnych z takich układów materiałowych wymaga głębokiego wejścia w zjawiska fizyko-chemiczne zachodzące na poziomie molekularnym. Z kolei przykładem aktywności naukowej w obszarze fundamentalnym są badania kinetyki przemian fazowych polimerów przebiegających w różnych warunkach zewnętrznych, np. w przestrzeni quasi-jednowymiarowej wewnątrz nanowłókien typu rdzeń-otoczka. Przykładem badań o dużym potencjale aplikacyjnym są badania dwuskładnikowych nanowłókien polimerowych formowanych metodą elektroprzędzenia z wykorzystaniem rozpuszczalników o małej toksyczności jako rusztowań do hodowli komórek. W ramach tego projektu opracowano w SPPiB procedurę formowania metodą elektroprzędzenia nanowłókien dwuskładnikowych polimer syntetyczny/biopolimer z wykorzystaniem alternatywnych, niedenaturujących rozpuszczalników o małej toksyczności. Opracowane procedury formowania pozwalają nie tylko na uzyskanie efektywnego materiału dla medycyny regeneracyjnej, ale również na obniżenie kosztów procesu ze względu na używanie stosunkowo tanich rozpuszczalników, a także istotne zmniejszenie uciążliwości procesu z perspektywy środowiska (ryc. 3).
 |
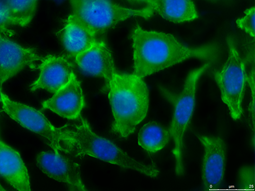 |
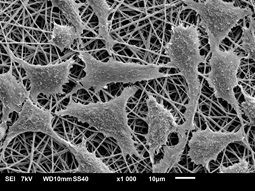
Ryc. 3. Fibroblasty linii L929 po 5 dniach hodowli na nanowłókninach polikaprolakton/żelatyna formowanych z wykorzystaniem alternatywnych rozpuszczalników. a) obraz ze skaningowego mikroskopu elektronowego; b) obraz z mikroskopu fluorescencyjnego
Przykładem prac o charakterze stricte aplikacyjnym jest projekt dotyczący opracowania membran z elektroprzędzonych nanowłókien do zastosowań w urologicznej medycynie regeneracyjnej. W SPPiB opracowano innowacyjne membrany kompozytowe wzbogacone w błonę owodniową jako czynnik przyspieszający gojenie, które zostały użyte do regeneracji ściany pęcherza moczowego na małym modelu zwierzęcym. Wykazano też możliwość otrzymywania mat z elektroprzędzonych nanowłókien bez zastosowania stałego podłoża – z użyciem wirującej powierzchni wody. W zakresie badań aplikacyjnych uzyskano w SPPiB szereg patentów, czego przykładem są patenty dotyczące innowacyjnych rusztowań komórkowych do zastosowań w regeneracji tkanki chrzęstnej, ośrodkowego układu nerwowego, układu krwionośnego oraz więzadeł.
Innym zadaniem nacelowanym na aplikacje są prace prowadzone w ramach konkursu Lider, finansowane ze środków NCBR, obejmujące opracowanie innowacyjnego, biodegradowalnego wyrobu medycznego do regeneracji więzadła kolanowego. Wyrób naśladuje architekturę i właściwości chemo-mechaniczne naturalnego więzadła i umożliwia proliferację, migrację i różnicowanie komórek. Po upływie określonego czasu materiał ulega biodegradacji w warunkach in-vivo, umożliwiając całkowitą regenerację więzadła naturalnego. Projekt ten jest prowadzony przy współudziale lekarzy-ortopedów z kliniki Ortopedika w Warszawie, Uniwersytetu Warszawskiego i Politechniki Warszawskiej.
SPPiB, będąc jednostką otwartą na zewnętrzną współpracę, prowadzi szereg wspólnych prac z partnerami z otoczenia zewnętrznego. Przykładem jest tu współpraca z kardiochirurgami z Wojskowego Instytutu Medycznego w Warszawie w zakresie opracowania innowacyjnego stentu zewnętrznego z polimerów biodegradowalnych do nakładania na naczynia krwionośne w czasie operacji pomostowania tętnic wieńcowych. Hamuje on skutecznie przerost ściany żyły zastosowanej jako pomost, wspomagając ponadto proces korzystnej przebudowy żyły w kierunku jej arterializacji oraz zabezpieczając pomost aortalno-wieńcowy przed zaginaniem, które mogło by ograniczać przepływ krwi przez naczynie żylne.
Zachęcamy do śledzenia strony internetowej SPPiB: http://polybiolab.ippt.pan.pl, gdzie znajdują się informacje o bieżącej aktywności SPPIB IPPT PAN.











